[NEJM] 화이자 & 바이오엔테크 COVID-19 백신(Pfizer-BioNTech BNT162b2 mRNA COVID-19 Vaccine) 임상결과 및 부작용 발표
Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine

미국 제약회사 화이자와 독일 생명공학기업 바이오엔테크(BioNTech SE)는 mRNA 기반 코로나19 백신 후보물질 ‘BNT162b2’의 임상 3상 시험에서 도출된 안전성 및 효능성 결과에 대해 의학 학술지 ‘뉴 잉글랜드 저널 오브 메디슨’(NEJM)에 게재됐다고 10일자로 발표했다.
이번 화이자 백신에 대한 임상시험연구는 16세이상 총 43,548명을 대상으로 다국적 무작위시험대조군(multinational, placebo-controlled, observer-blinded) 설계로 진행되었다. 백신투여군과 위약투여군을 무작위로 1:1로 배정하여 임상실험을 수행하였다.

이들 가운데 백신후보군 21,720명에게 ‘BNT162b2’ 30μg을 21일 간격으로 2회 투여하였던 반면, 21,728명은 위약 플라시보를 2회 투여했다.
BNT162b2 백신 부작용
연령, 성별, 인종, 민족성, BMI 및 유사한 조건의 동질성에 대한 베이스라인의 하위그룹에서 유사한 백신효능(일반적으로 90~100%)과 부작용이 관찰되었다. 연구에 등록된 모든 43,252명의 참가자에 대한 부작용에 대한 분석이 이루어졌다.
위약실험군보다 BNT162b2 백신 투여군에서 좀 더 높은 부작용반응 (27 % vs. 12 %), 또는 관련 이상 반응 (21 % vs. 5%)을 보고했다. 이 분포는 대체로 위약 투여군보다 백신 투여군에서 더 흔하게 이상 반응으로 보고되는 일시적인 반응 원성양상을 반영하고 있다. 64명의 백신투여군과 6명의 위약투여군 (0.3% vs. <0.1 %)가 림프절병증을보고했다. 두 그룹 모두 중증이상반응, 중대이상반응 또는 임상시험중단으로 이어지는 심각한 이상반응을 경험한 참가자는 거의 없었다. 다만 BNT162b2 투여군 중 4 건에서 의 심각한 부작용이 (백신투여와 관련된 어깨 손상, 오른쪽 겨드랑이 림프절병증, 발작성 심실부정맥 및 오른쪽 다리 감각 이상)등이 보고되었다. BNT162b2에 대한 안정성 프로필은 주사부위의 경증 중등도의 단기적 통증, 피로감, 두통, 메스꺼움, 불쾌감 등이 관찰되었다.
최근 영국 의료진에서 화이자백신을 접종받은 이후 중증 알레르기 반응을 경험한 사례들이 몇건 보고되었는데, FDA는 화이자 백신의 성분에 '아나필락시스(anaphylaxis)' 반응, 즉 심각한 알레르기 반응이 보고되었으므로 알레르기 반응에 대한 주의를 당부하였다. 아나필락틱 쇼크는 항원-항체 면역반응 때문에 발생하는 급격한 전신반응으로, 이는 사람이 어떠한 물질에 노출된 이후 혈압이 급격히 감소하거나 호흡곤란을 겪는 등 치명적일 수 있는 중증 알레르기 반응이다. 그외 백신 투여 후에 사망자로는 BNT162b2 투여군 중에서 2 명 (1명은 동맥경화증, 1명은 심장마비)과 위약 투여군 중 4명(2명은 원인불명, 1명은 출혈성 뇌졸중, 1명은 심근경색)이 보고되었으나, 연구조사관은 백신 또는 위약과 관련된 사망으로 간주하지 않았다. Covid-19 감염으로 으로 인한 사망은 연구기관 동안 관찰되지 않았다. 즉, BNT162b2 투여군에서 심각한 부작용은 보고되지 않았고 이는 위약군과 유사한 결과임은 연구는 보고했다.
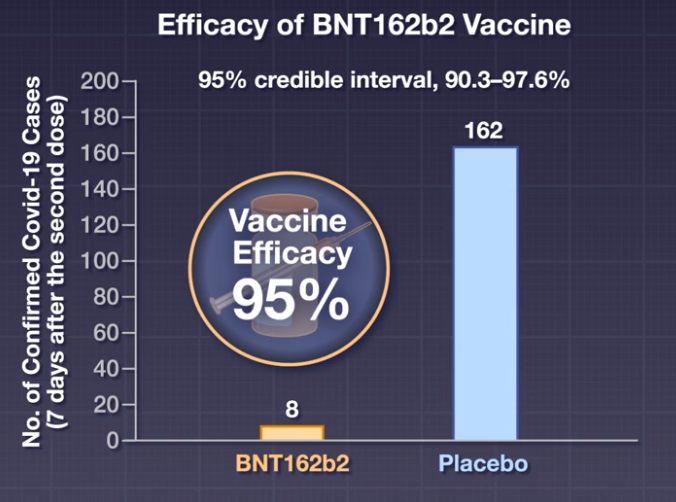
결론적으로 양호한 내약성을 나타낸 가운데 화이자와 바이오엔테크사가 개발한 COVID-19 예방백신, BNT162b2는 ‘COVID-19 예방에 95%에 달하는 효과가 있는 것으로 연구결과를 보고했다(95% CI, 90.3- 97.6).
미국 FDA는 COVID-19 백신에 대한 긴급사용승인(EUA)을 하면서 화이자와 바이오엔테크사(THE PFIZER-BIONTECH COVID-19 VACCINE)가 개발한 COVID-19 백신에 대한 의료인들을 위한 COVID-19 백신투여에 대한 Fact Ssheet를 배포하였다. 화이자도 부작용에 대한 보고를 할 수 있도록 국가별로 웹사이트를 통해 등록할 수 있도록 조치하였다. 향후 안전에 대한 모니터링은 두번째 백신투여 후, 2 년 동안 지속 될 예정이다. 결론적으로 화이자가 개발한 COVID-19 백신 ‘BNT162b2’의 2회 투여요법은 16 세 이상의 사람들에게 Covid-19 예방에 95 % 보호효과를 나타내었다. (Funded by BioNTech and Pfizer; ClinicalTrials.gov number, NCT04368728. opens in new tab).


의과학연구정보센터 제공
Reference
Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine (2020). The New England Journal of Medicine. December 10, 2020. DOI: 10.1056/NEJMoa2034577.
FACT SHEET FOR HEALTHCARE PROVIDERS ADMINISTERING VACCINE (VACCINATION PROVIDERS) URL: https://www.fda.gov/media/144413/download
Global Information About Pfizer?BioNTech COVID?19 Vaccine (also known as BNT162b2)URL: https://www.cvdvaccine.com/
Pfizer safety reporting URL: https://www.pfizersafetyreporting.com/